
Químicos Curie



Ácidos y bases de Lewis
.jpg)

En 1923, GN Lewis propuso una definición generalizada del comportamiento ácido-base en la que los ácidos y las bases se identifican por su capacidad de aceptar o donar un par de electrones y formar un enlace covalente coordinado.
Un símbolo de los puntos de Lewis representa un punto por cada electrón de valencia de un elemento de la tabla periódica. Los representamos como:

El número de electrones de valencia es el mismo que el número del grupo en que está el elemento en la tabla periódica
Estructuras de Lewis

La unión de dos electrones de diferentes elementos representa un enlace, por ejemplo,
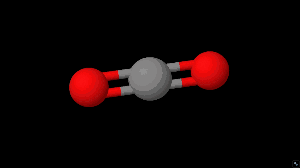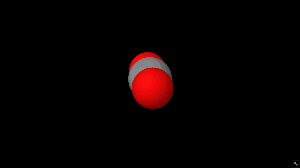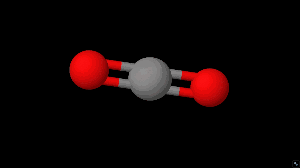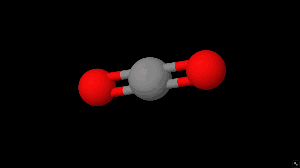
Estructura de Lewis del CO2
La molécula tiene:
• 4 enlaces en total.
• 2 dobles enlaces.
• 4 pares de electrones libres.

.png)
La estructura, donde la esfera negra es el carbono y las rojas los oxígenos:
